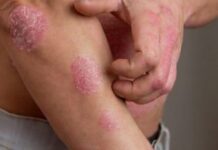
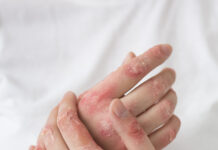
A Food and Drug Administration (FDA) autorizou na sexta-feira a vacinação contra o COVID-19 pela primeira vez para crianças de cinco anos de idade ou menos.
Cerca de 18 milhões de crianças em idade pré-escolar podem começar já na próxima semana.
A mudança significa que todas as crianças entre seis meses e 17 anos de idade podem receber qualquer uma das opções de vacina, aproximadamente um ano e meio após a primeira aprovação para uso adulto.
“Muitos pais, cuidadores e médicos estão esperando por uma vacina para crianças mais novas e por essa ação”, disse o comissário da FDA, Robert Califf, em comunicado na sexta-feira. “Como vimos com grupos etários mais velhos, esperamos que as vacinas para crianças mais novas forneçam proteção contra os resultados mais graves do COVID-19, como hospitalização e morte”.
O anúncio de sexta-feira ocorre cerca de uma semana depois que a FDA autorizou a vacina Moderna para crianças de seis a 17 anos, enquanto apenas a Pfizer havia sido aprovada anteriormente para crianças em idade escolar.
Os consultores de vacinas dos Centros de Controle e Prevenção de Doenças (CCP) discutirão e votarão em seguida as melhores práticas para administrar as vacinas aos pacientes mais jovens do país.
Espera-se que a aprovação final da aprovação da vacina venha do diretor do CDC, Dr. Rochelle Walensky, no sábado.
A diretora disse aos legisladores durante uma audiência no Senado na quinta-feira que ela e sua equipe trabalharão durante o feriado federal de Juneteeth “porque entendemos a urgência disso para os pais americanos”.
Walensky disse que o número de mortes pediátricas pelo vírus – que atormentou em grande parte adultos e idosos no ataque da pandemia – tendeu a ser mais alto do que os números vistos na gripe.
“Na verdade, acho que precisamos proteger as crianças pequenas, bem como proteger todos com a vacina e, especialmente, proteger os idosos”, disse ela.